Ribosomen in Aktion
Ein dreidimensionales Bild eines aktiven Proteins oder Protein-Komplexes zu erstellen, stellt Forscher vor ein schwer zu lösendes Problem: Der Aufbau der Makromoleküle ist nicht nur sehr kompliziert, sondern die Moleküle sind zudem ständig in Bewegung und können dabei verschiedene räumliche Anordnungen einnehmen. Diese sogenannten Konformationen sind von grundlegender Bedeutung für die Aktivität und Funktion eines Proteins. Um den räumlichen Aufbau von Proteinen zu untersuchen, müssen die Moleküle bislang chemisch fixiert werden, oft mit Giftstoffen oder Antibiotika. Der Nachteil dieser Methode: Die Chemikalien können die Struktur des Proteins beeinflussen, die dann eventuell nicht mehr einer funktionell relevanten Konformation entspricht. Wissenschaftler der Charité – Universitätsmedizin Berlin und des Bonner Forschungszentrums caesar, einem Institut der Max-Planck-Gesellschaft, haben jetzt eine neue Methode angewendet, um die Struktur von Protein-Komplexen im aktiven Zustand zu untersuchen. Dafür haben die Forscher eine Probe mit menschlichen Polysomen – also Ribosomen, die zur Protein-Synthese an einem mRNA-Molekül aufgereiht sind – in flüssigem Ethan schockgefroren. Ihre dreidimensionale Struktur haben sie anschließend mittels Kryo-Elektronenmikroskopie rekonstruiert.
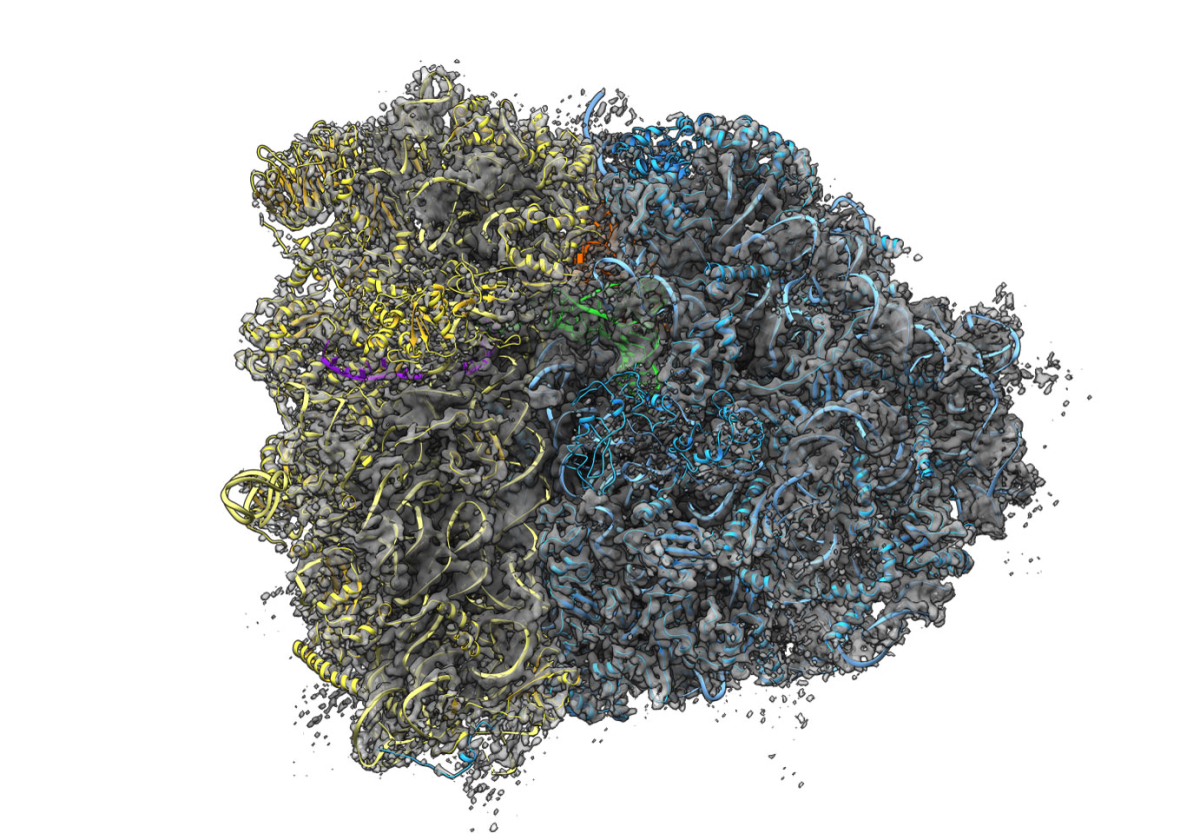
Mithilfe eines rechenintensiven mathematischen Algorithmus konnten die Wissenschaftler insgesamt elf – teilweise bislang unbekannte – funktionelle Zustände identifizieren. Zudem erstellten sie das erste hochaufgelöste atomare Modell eines aktiven menschlichen Ribosoms. Ein solch detaillierter Bauplan hilft dabei, die Funktion der Ribosomen besser zu verstehen und könnte so die Entwicklung von neuartigen Medikamenten unterstützen. "Faszinierend an der Studie ist nicht nur, dass wir eine Vielzahl unterschiedlicher Konformationen des menschlichen Ribosoms gleichzeitig abbilden können, sondern auch, dass wir Bilder von realen Zuständen aus der Zelle erhalten", sagt Justus Loerke vom Institut für Medizinische Physik und Biophysik der Charité. Sein Kollege Elmar Behrmann, der mittlerweile als Freigeist-Fellow der VolkswagenStiftung eine Arbeitsgruppe am Bonner Forschungszentrum caesar leitet, ergänzt: "Aktive Proteine sind in der Regel in Bewegung. Um ihre Struktur zu ermitteln, werden sie häufig inaktiviert. Dieses ist bei unserem Ansatz nicht der Fall. Allerdings musste die Probe zur Vorbereitung eingefroren werden, es fehlt uns also eine zeitliche Auflösung der verschiedenen Zustände." Wie sich diese zeitliche Dynamik von Proteinen untersuchen lässt, erforscht Behrmann derzeit im Rahmen eines Freigeist-Fellowships der VolkswagenStiftung. Genauere Informationen zu seiner Forschungsarbeit gibt Behrmann im Interview unter "Tanzende Proteine verstehen".
Originalpublikation
*Behrmann E, Loerke J, Budkevich TV, Yamamoto K, Schmidt A, Penczek PA, Vos MR, Bürger J, Mielke T, Scheerer P, Spahn CM. Structural snapshots of actively translating human ribosomes. Cell. 2015 May 7;161(4):845-57. doi: 10.1016/j.cell.2015.03.052. PubMed PMID: 25957688.
Weitere Informationen zur Publikation finden Sie unter http://biophysik.charite.de/.
Hintergrund: Freigeist-Fellowships
Die fachoffenen Freigeist-Fellowships der VolkswagenStiftung richten sich an außergewöhnliche Forscherpersönlichkeiten mit bis zu fünfjähriger Forschungserfahrung nach der Promotion, die sich zwischen etablierten Forschungsfeldern bewegen und risikobehaftete Wissenschaft betreiben möchten. Der nächste Stichtag ist der 15. Oktober 2015. Weitere Informationen unter "Freigeist-Fellowships".

